








جمعية تكنولوجيا الهندسة الطبية
02/07/2024
هندسة الطباعة الحيوية ثلاثية الأبعاد لطباعة الأنسجة والأعضاء: هندسة المستقبل
خلاصة:
تُعتبر الطباعة الحيوية ثلاثية الأبعاد واحدة من أكثر الابتكارات التكنولوجية إثارةً في مجال الطب الحيوي الحديث. هذه التقنية، التي تجمع بين الطباعة ثلاثية الأبعاد والتكنولوجيا الحيوية، تُتيح إمكانية طباعة أنسجة وأعضاء بشرية باستخدام خلايا جذعية وأحبار حيوية مصممة خصيصًا. من خلال هذا المقال، نستعرض تفاصيل ماهية الطباعة الحيوية ثلاثية الأبعاد، ونفرق بينها وبين الطباعة ثلاثية الأبعاد التقليدية، ونلقي الضوء على أنواع الأحبار الحيوية والطابعات المستخدمة في هذا المجال. كما نتناول الأنسجة والأعضاء التي تمت طباعتها بنجاح حتى الآن، ونتحدث عن التحديات الحالية التي تواجه هذا المجال، بالإضافة إلى استعراض التوجهات المستقبلية لهذه التكنولوجيا الثورية.

فقرة. 1: طابعة حيوية ثلاثية ابعاد اثناء عملية طباعة عضو القلب. الحقوق محفوظة لاندريو بروهيد – جامعة ستانفورد
مقدمة:
تعتبر الطباعة ثلاثية الأبعاد واحدة من التقنيات الحديثة التي أحدثت ثورة في العديد من الصناعات، بما في ذلك الطب والهندسة1. ولكن عندما نتحدث عن الطباعة الحيوية ثلاثية الأبعاد، فإننا نشير إلى استخدام هذه التكنولوجيا لطباعة أنسجة وأعضاء بشرية باستخدام مواد هلامية وخلايا حية2. هذا المجال الناشئ يقدم وعودًا هائلة لتحسين نوعية الحياة للمرضى من خلال تقديم حلول مبتكرة لتعويض الأنسجة والأعضاء التالفة أو المفقودة (الفقرة. 1). وتكمن أهمية الطباعة الحيوية ثلاثية الأبعاد في قدرتها على:
ما هي الطباعة الحيوية ثلاثية الأبعاد؟
الطباعة الحيوية ثلاثية الأبعاد هي تقنية متقدمة تستخدم لطباعة أنسجة وأعضاء حية باستخدام خلايا حية ومواد حيوية أخرى3. تعتمد هذه التقنية على مبادئ الطباعة ثلاثية الأبعاد التقليدية، حيث يتم بناء الجسم المراد طباعته طبقةً فوق طبقة باستخدام طابعات ثلاثية الأبعاد مصممة خصيصًا لهذا الغرض. تشمل عملية الطباعة الحيوية خطوات رئيسية تبدأ بتصميم نموذج رقمي ثلاثي الأبعاد للنسيج أو العضو المطلوب باستخدام برامج التصميم بمساعدة الحاسوب (CAD)، والذي يمكن الحصول عليه من خلال تقنيات التصوير الطبي مثل التصوير بالرنين المغناطيسي (MRI) أو التصوير المقطعي المحوسب (CT). بعد ذلك، يتم إعداد "الحبر الحيوي" الذي يتكون من خلايا حية ومواد هلامية (هيدروجيل) وعوامل نمو، حيث توفر هذه المواد الدعم للخلايا وتساعدها على النمو والتطور بشكل صحيح. ثم يتم استخدام الطابعة الحيوية ثلاثية الأبعاد لبناء النسيج أو العضو طبقةً فوق طبقة، مما يمكن العلماء والأطباء من إنتاج أنسجة وأعضاء معقدة يمكن استخدامها في الأبحاث الطبية والعلاج. هذه التقنية تفتح آفاقًا جديدة في مجال الطب التجديدي وزراعة الأعضاء، مما قد يسهم في تحسين العلاجات الطبية وإنقاذ حياة الكثير من المرضى3.
ما هو الفرق بين الطباعة ثلاثية الأبعاد والطباعة الحيوية ثلاثية الأبعاد؟
الفرق بين الطباعة ثلاثية الأبعاد والطباعة الحيوية ثلاثية الأبعاد يكمن في المواد المستخدمة والأغراض المستهدفة لكل منهما. الطباعة ثلاثية الأبعاد التقليدية تستخدم مواد مثل البلاستيك، المعادن، أو الراتنج لبناء نماذج صلبة ثلاثية الأبعاد من طبقات متتالية، وتُستخدم بشكل واسع في الصناعات التحويلية، الهندسة، التصميم، وصناعة النماذج الأولية. من ناحية أخرى، الطباعة الحيوية ثلاثية الأبعاد تعتمد على استخدام خلايا حية ومواد حيوية هلامية مثل الهيدروجيل لبناء أنسجة وأعضاء بيولوجية. بينما تركز الطباعة ثلاثية الأبعاد التقليدية على إنشاء هياكل صلبة وغير حية، تهدف الطباعة الحيوية إلى إنشاء هياكل حية يمكن أن تنمو وتتكامل مع الجسم البشري. علاوة على ذلك، تتطلب الطباعة الحيوية دقة أكبر في التعامل مع المواد الحساسة والحفاظ على الظروف البيئية المثلى لنمو الخلايا. ايضا، تختلف الطابعات الحيوية في تصميمها وطريقة عملها عن الطابعات ثلاثية الأبعاد التقليدية، حيث أنها مُصممة لتلبية متطلبات معينة مثل التوافق الحيوي وتوفير بيئة معقمة لنمو الخلايا. لذلك، نجد ان الطابعات الحيوية ثلاثية الابعاد دائما ما توضع بداخل صناديق لديها القدرة على توليد تدفق هوائي طبقي للحفاظ على البيئة المعقمة داخل الطابعة (فقرة. 2).
وهكذا، تهدف الطباعة الحيوية ثلاثية الابعاد إلى تطبيقات طبية حيوية مثل زراعة الأنسجة والأعضاء، ودراسة الأمراض، واختبار الأدوية. فعلى الرغم من تشابه التقنيات الأساسية، إلا أن الأهداف والمواد المستخدمة في كل منهما تجعلها تلبي احتياجات واستخدامات مختلفة تمامًا.

فقرة. 2: أحدث الطابعات الحيوية ثلاثية الابعاد من شركة CELLINK. يلاحظ ان الطابعة مغلقة تماما للحفاظ على البيئة المعقمة بالداخل.
الأحبار الحيوية للطباعة الحيوية ثلاثية الأبعاد
الأحبار الحيوية للطباعة الحيوية ثلاثية الأبعاد هي مواد حيوية تُستخدم لبناء أنسجة وأعضاء حية باستخدام تقنية الطباعة الحيوية ثلاثية الأبعاد. تتكون هذه الأحبار من خلايا حية، مواد هلامية (هيدروجيل)، وعوامل نمو، وغيرها من المواد الحيوية التي تدعم نمو وتطور الخلايا4.
الهيدروجيل هو المكون الأساسي للأحبار الحيوية، وهو مادة بوليمرية تتميز بقدرتها على الاحتفاظ بكميات كبيرة من الماء، مما يوفر بيئة رطبة وداعمة للخلايا. يمكن تعديل خصائص الهيدروجيل من حيث التركيب الكيميائي والفيزيائي لتتناسب مع نوع الخلايا والنسيج المراد طباعته.
تُضاف الخلايا الحية إلى الهيدروجيل لتكوين الحبر الحيوي، بحيث تكون الخلايا مغمورة داخل الهيدروجيل وتتمكن من النمو والتكاثر ضمن الهيكل المطبوع. تشمل هذه الخلايا خلايا جذعية، خلايا نسيجية متخصصة، أو خلايا مبرمجة حسب الحاجة.
بالإضافة إلى الهيدروجيل والخلايا، يمكن أن تحتوي الأحبار الحيوية على عوامل نمو وبروتينات تنظيمية تحفز نمو الخلايا وتمايزها وتوجهها لتكوين الأنسجة الصحيحة. كما يمكن أن تُضاف مواد داعمة أخرى لتحسين استقرار الهيكل المطبوع وزيادة توافقه الحيوي.
توجد هناك عدة أنواع من الأحبار الحيوية التي تم استخدامها لهذا الغرض، منها:
الهيدروجيلات الطبيعية: مثل الجيلاتين، الكولاجين، والألجينات. هذه المواد تتميز بقدرتها على محاكاة البيئة الطبيعية للخلايا، مما يساعد على تعزيز نمو الخلايا وتمايزها.
الهيدروجيلات الاصطناعية: مثل بولي إيثيلين جلايكول (PEG) والبولي أكريلاميد. هذه المواد تسمح بتحكم دقيق في الخصائص الفيزيائية والكيميائية للحبر الحيوي.
الأحبار الحيوية القائمة على الخلايا الجذعية: حيث يتم استخدام خلايا جذعية متعددة القدرات يمكن أن تتمايز إلى أنواع مختلفة من الخلايا حسب الحاجة.
الأحبار الحيوية المختلطة: التي تجمع بين الهيدروجيلات الطبيعية والاصطناعية لتحقيق توازن بين الخصائص البيولوجية والميكانيكية.
تعتبر الأحبار الحيوية جزءًا أساسيًا في عملية الطباعة الحيوية ثلاثية الأبعاد، حيث تلعب دورًا حيويًا في تحقيق الهدف النهائي من إنتاج أنسجة وأعضاء حية قابلة للاستخدام في التطبيقات الطبية والعلاجية.
كيف تتم عملية الطباعة ثلاثية الابعاد؟
تبدأ العملية بإنشاء نموذج رقمي ثلاثي الأبعاد للنسيج أو العضو المراد طباعته باستخدام برامج التصميم بمساعدة الحاسوب (CAD)، ويمكن الحصول على هذا النموذج من خلال تقنيات التصوير الطبي مثل التصوير بالرنين المغناطيسي (MRI) أو التصوير المقطعي المحوسب (CT)5. يتكون الحبر الحيوي من خلايا حية ومواد هلامية (هيدروجيل) وعوامل نمو، حيث تُختار الخلايا المناسبة للنسيج المطلوب وتُمزج مع الهيدروجيل الذي يوفر بيئة رطبة وداعمة للخلايا. بعد إعداد الطابعة الحيوية ثلاثية الأبعاد، تبدأ الطباعة داخل حمام داعم تضحيحي، حيث يوفر هذا الحمام الدعم الهيكلي اللازم لبناء النسيج أو العضو طبقةً فوق طبقة بناءً على التصميم الرقمي. بعد الطباعة، يتم التخلص من الحمام الداعم التضحيحي ويُوضع النسيج أو العضو المطبوع في حاضنة بيولوجية توفر الظروف المثالية لنمو الخلايا وتكاثرها، مع إضافة عوامل نمو ومكونات غذائية لدعم عملية النضوج والتكامل الخلوي. بمجرد نضوج النسيج أو العضو، يتم اختباره لضمان وظيفته وسلامته، وإذا كانت النتائج مرضية، يمكن استخدامه في الأبحاث أو زراعته في المرضى الذين يحتاجون إلى تجديد أنسجة أو أعضاء.
أنواع الطابعات الحيوية ثلاثية الأبعاد
هناك عدة أنواع من الطابعات الحيوية ثلاثية الأبعاد التي تختلف في آليات عملها والتطبيقات المستهدفة (فقرة. 3). تشمل الأنواع الرئيسية الطابعات النفاثة للحبر الحيوي، التي تعتمد على تقنية نفث الحبر لطرد الحبر الحيوي على شكل قطرات صغيرة من خلال فوهات دقيقة، مما يجعلها مفيدة للطباعة السريعة والدقيقة للأنسجة ذات التراكيب المعقدة. وهناك الطابعات البثق الحيوي، التي تستخدم تقنية البثق لوضع الحبر الحيوي بشكل مستمر عبر فوهة، مما يسمح بطباعة هياكل ثلاثية أبعاد معقدة وداعمة للخلايا. بالإضافة إلى ذلك، توجد الطابعات الضوئية الحيوية التي تعتمد على تقنية البلمرة الضوئية، حيث يتم استخدام الضوء لربط جزيئات الحبر الحيوي وتشكيل الهياكل بشكل دقيق. هذه الطابعات قادرة على تحقيق دقة عالية في بناء الأنسجة والأعضاء. كل نوع من هذه الطابعات يتميز بخصائص معينة تجعله مناسبًا لتطبيقات محددة في مجال الطب التجديدي والبحوث العلمية.
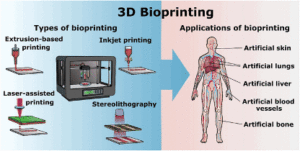
فقرة. 3: أنواع الطابعات الحيوية ثلاثية الابعاد6.
الأنسجة التي تمت طباعتها بنجاح
تمكنت الطباعة الحيوية ثلاثية الأبعاد من تحقيق نجاحات ملحوظة في طباعة العديد من الأنسجة، مما يعزز آفاق الطب التجديدي. تشمل الأنسجة التي تمت طباعتها بنجاح أنسجة الغضاريف7، حيث تمكن العلماء من طباعة غضاريف مفاصل الركبة والفك بنجاح، مما يفتح المجال لعلاج الإصابات والتآكل الغضروفي. كذلك، تم طباعة أنسجة الجلد باستخدام خلايا جلدية بشرية، مما يسهم في تطوير علاجات جديدة للحروق والجروح العميقة8. بالإضافة إلى ذلك، تمت طباعة أنسجة الأوعية الدموية9، حيث تم تصنيع شرايين وأوردة صغيرة بنجاح، وهو ما يمكن أن يكون له تأثير كبير في جراحات القلب وزراعة الأعضاء. كما شهدت الأبحاث تطورات في طباعة أنسجة الكبد والكلى، حيث تم إنشاء نماذج أولية صغيرة يمكن استخدامها في اختبارات الأدوية والأبحاث الطبية. علاوة على ذلك، تم وبكل نجاح طباعة انسجة عضلية هيكلية يمكنها أداء الوظائف المخصصة للعضلات وهي الانقباض الانبساط، والتي ساهمت في توفير حلول لفاقدي العضلات10. هذه النجاحات تؤكد الإمكانيات الكبيرة للطباعة الحيوية في تجديد الأنسجة التالفة وزراعة الأعضاء، مما يعزز الأمل في تحسين جودة الحياة للمرضى الذين يعانون من أمراض وإصابات خطيرة.
الأعضاء التي تمت طباعتها بنجاح
لقد حققت الطباعة الحيوية ثلاثية الأبعاد نجاحات ملحوظة في طباعة العديد من الأعضاء التي قد تكون لها تطبيقات واسعة في الطب التجديدي. من بين الأعضاء التي تمت طباعتها بنجاح، الكبد المصغر، حيث استطاع العلماء طباعة نماذج أولية من أنسجة الكبد القادرة على أداء وظائف حيوية بسيطة11، مما يفتح الباب لاختبارات الأدوية ودراسة الأمراض الكبدية. كما تم طباعة قلوب مصغرة تحتوي على خلايا عضلية قادرة على النبض بشكل طبيعي12، مما يعتبر خطوة مهمة نحو تطوير قلب كامل قابل للزرع في المستقبل.
بالإضافة إلى ذلك، تم طباعة أنسجة الكلى المصغرة التي يمكن استخدامها في دراسات وظائف الكلى واختبار الأدوية13. كما شهدت الأبحاث تقدمًا في طباعة أجزاء من الرئة14، مما يساعد في دراسة الأمراض التنفسية وتطوير علاجات جديدة. أيضًا، نجحت الطباعة الحيوية في إنتاج هياكل معقدة مثل الأذنين والأنف15، التي يمكن استخدامها في الجراحات التجميلية والتعويضية.
التحديات الحالية في مجال الطباعة الحيوية ثلاثية الأبعاد
على الرغم من التقدم الكبير الذي تحقق في مجال الطباعة الحيوية ثلاثية الأبعاد، إلا أن هناك العديد من التحديات التي لا تزال تواجه هذا المجال الواعد. أحد أبرز التحديات هو ضمان بقاء الخلايا حية وقادرة على العمل بشكل طبيعي أثناء وبعد عملية الطباعة، حيث يتطلب ذلك بيئة دقيقة تحافظ على درجة الحرارة والرطوبة والتغذية المناسبة للخلايا.
التحدي الآخر يكمن في تطوير أحبار حيوية مثالية، حيث يجب أن تكون هذه الأحبار متوافقة حيويًا وقادرة على دعم نمو وتمايز الخلايا بشكل فعال. بالإضافة إلى ذلك، تتطلب الطباعة الحيوية ثلاثية الأبعاد دقة عالية في وضع الطبقات الخلوية والمواد الحيوية، مما يجعل التحكم في الطابعات وتطوير تقنيات طباعة دقيقة ومعقدة أمرًا ضروريًا.
من التحديات الأخرى هو تكرار التعقيد البنيوي والوظيفي للأعضاء الطبيعية، إذ تتطلب الأعضاء البشرية تعقيدًا كبيرًا في تكوينها وتشابكها لتعمل بشكل صحيح. هذا يتطلب فهمًا عميقًا للهندسة البيولوجية والقدرة على تصنيع هياكل معقدة ومتكاملة.
كما تواجه الطباعة الحيوية تحديات تنظيمية وأخلاقية، حيث يجب التأكد من أن الأنسجة والأعضاء المطبوعة آمنة وفعالة للاستخدام البشري، وهو ما يتطلب تجارب واختبارات طويلة الأمد بالإضافة إلى موافقات من الهيئات الصحية والتنظيمية.
أخيرًا، التحدي المالي يعد من العوائق الكبيرة، حيث إن تقنيات الطباعة الحيوية تحتاج إلى استثمارات ضخمة في البحث والتطوير، ما يجعلها غير متاحة على نطاق واسع في الوقت الحالي.
تجاوز هذه التحديات يتطلب جهودًا متضافرة من الباحثين، المهندسين، الأطباء، والهيئات التنظيمية، بالإضافة إلى الدعم المالي المستدام لتسريع التقدم في هذا المجال الحيوي والمهم.
الخلاصة والتوجهات المستقبلية
في الخلاصة، تُعتبر الطباعة الحيوية ثلاثية الأبعاد تقنية مبتكرة تحمل إمكانيات هائلة في مجال الطب التجديدي، مما يفتح آفاقًا جديدة في علاج الأمراض وزراعة الأعضاء. على الرغم من التحديات الكبيرة التي تواجه هذا المجال، مثل ضمان بقاء الخلايا حية، وتطوير أحبار حيوية متوافقة، وتحقيق التعقيد البنيوي والوظيفي للأعضاء، والتحديات التنظيمية والأخلاقية والمالية، فإن التقدم المستمر في التكنولوجيا والأبحاث يساهم في التغلب على هذه العقبات تدريجيًا.
التوجهات المستقبلية في مجال الطباعة الحيوية ثلاثية الأبعاد تشمل تحسين دقة وكفاءة تقنيات الطباعة، وتطوير مواد حيوية جديدة وأكثر تطورًا لدعم نمو الخلايا بشكل أفضل، بالإضافة إلى التركيز على إنتاج أعضاء وأنسجة أكثر تعقيدًا وقادرة على أداء وظائفها الحيوية بكفاءة. كما يتوقع أن يشهد المجال تقدمًا في استخدام الذكاء الاصطناعي وتعلم الآلة لتحسين تصميم النماذج الرقمية وتحسين عمليات الطباعة.
تتجه الأبحاث أيضًا نحو تحقيق الطباعة الحيوية الشخصية، حيث يمكن تصميم الأنسجة والأعضاء المطبوعة لتتناسب مع الاحتياجات الفردية للمرضى، مما يزيد من فرص النجاح في عمليات الزراعة ويقلل من مخاطر الرفض المناعي. بالإضافة إلى ذلك، يُتوقع أن تُستخدم الطباعة الحيوية في تطوير نماذج دقيقة للأمراض البشرية، مما يسهم في تحسين فهمنا للأمراض وتطوير علاجات جديدة.
في النهاية، مستقبل الطباعة الحيوية ثلاثية الأبعاد مشرق ومحفوف بالإمكانيات التي يمكن أن تغير وجه الطب والعلاج البشري، مما يجعلها مجالًا حيويًا يستحق الاستمرار في الاستثمار والبحث لتقديم حلول مبتكرة ومستدامة للمشاكل الصحية المعقدة.
المراجع: